使用目的に沿って適正に使用されている状況で副作用や機能障害などの不具合が生じた場合、人の生命および健康に重大な影響を与えるおそれがあり、その適切な管理が必要とされる医療機器。クラス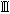 (不具合が生じると人体へのリスクが比較的高い)とクラス
(不具合が生じると人体へのリスクが比較的高い)とクラス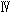 (人体への侵襲性が高く、不具合が生じると生命の危険に直接結び付くおそれがある)に分類される。クラスは、厚生労働大臣により薬事・食品衛生審議会の意見を聴取したうえでさまざまな医療機器が指定され、随時見直しが行われている。クラス
(人体への侵襲性が高く、不具合が生じると生命の危険に直接結び付くおそれがある)に分類される。クラスは、厚生労働大臣により薬事・食品衛生審議会の意見を聴取したうえでさまざまな医療機器が指定され、随時見直しが行われている。クラス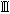 には、透析器、人工骨頭、 人工呼吸器、汎用(はんよう)輸液ポンプ、放射線治療機器などが含まれ、クラス
には、透析器、人工骨頭、 人工呼吸器、汎用(はんよう)輸液ポンプ、放射線治療機器などが含まれ、クラス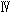 には、ペースメーカー、中心静脈用カテーテル、人工心臓弁、ステントグラフトなどが含まれる。
には、ペースメーカー、中心静脈用カテーテル、人工心臓弁、ステントグラフトなどが含まれる。
2002年(平成14)の薬事法改正により、それまでの医療用具は医療機器に名称変更された。医療機器は、人体に及ぼすリスクの程度に応じて必要な安全策を講じる目的で、国際分類などに沿って高度管理医療機器(クラス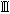 、
、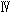 。不具合が生じれば生命の危険や健康へ影響を及ぼすリスクが高い)、管理医療機器(クラス
。不具合が生じれば生命の危険や健康へ影響を及ぼすリスクが高い)、管理医療機器(クラス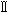 。不具合が生じても人体へのリスクが比較的少ない)、一般医療機器(クラス
。不具合が生じても人体へのリスクが比較的少ない)、一般医療機器(クラス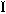 。不具合が生じても人体へのリスクがきわめて少ない)の三つに分類され、それぞれ承認や販売に関する規定が設けられた。
。不具合が生じても人体へのリスクがきわめて少ない)の三つに分類され、それぞれ承認や販売に関する規定が設けられた。
これら機器の製造販売は厚生労働大臣の承認が必要であったが、2014年の医薬品医療機器等法の成立により、クラス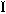 ~
~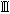 の医療機器は独立行政法人医薬品医療機器総合機構(PMDA:Pharmaceuticals and Medical Devices Agency)や公益財団法人医療機器センター(JAAME:Japan Association for the Advancement of Medical Equipment)など民間の第三者登録認証機関(RCB:Recognized Certification Body)で基準に適合していると認証(第三者認証)されるだけで可能になった。クラス
の医療機器は独立行政法人医薬品医療機器総合機構(PMDA:Pharmaceuticals and Medical Devices Agency)や公益財団法人医療機器センター(JAAME:Japan Association for the Advancement of Medical Equipment)など民間の第三者登録認証機関(RCB:Recognized Certification Body)で基準に適合していると認証(第三者認証)されるだけで可能になった。クラス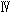 は、厚生労働大臣の承認が必要で、また販売にあたってはPMDAの認証が必要である。
は、厚生労働大臣の承認が必要で、また販売にあたってはPMDAの認証が必要である。
こうしたクラス分類にかかわらず、保管や修理などに専門的な知識と技術を要する医療機器は特定保守管理医療機器として扱われ、また設置にあたって組立てを要し、保健衛生上の危害発生を防ぐ目的で設置に管理を必要とする医療機器を設置管理医療機器とよぶ。
さらに医療機器の申請にあたっては、新たに開発された新医療機器、従来のものに改良を加えた改良医療機器、すでに承認された医療機器と同等の効果や効能が認められる後発医療機器などの区分があり、安全性と効能を明らかにできる臨床試験データの提出が必要なものと不要なものとがある。申請者は第一種医療機器製造販売業許可を取得している必要がある。
[編集部]